屏幕上,一個細胞正在慢慢變大。它只有幾百納米寬,肉眼完全不可見,但在模擬畫面裏被放大到可以看清內部的一切:蛋白質、RNA、核糖體密密麻麻地擠在一起。一條環形染色體蜷縮在中央,正在被複制。
到第 65 分鐘前後,細胞開始變形,腰部收窄,拉成啞鈴的形狀。第 105 分鐘,兩個子細胞徹底分開,各自帶走了一套完整的染色體,以及大約一半的核糖體、蛋白質和 RNA。

(來源:Youtube)
這看起來是不是像一段手搓的虛擬 3D 動畫?但它不是,它是兩塊 GPU 跑了 6 天的計算結果,裏面每一個分子的每一步移動,都是計算機算出來的。
2026 年 3 月,美國伊利諾伊大學厄巴納-香檳分校(UIUC)化學系教授 Zaida Luthey-Schulten 領銜的團隊在 Cell 期刊上發表了這項工作。他們構建了一個四維全細胞模型(4DWCM,即三維空間加時間維度),完整模擬了已知基因組最小的自由生活細菌 JCVI-syn3A 從"出生"到一分爲二的整個生命週期——大約 105 分鐘。這是人類第一次在計算機中讓一個細胞"活"過完整的一生,而且每一步都符合真實的生物物理規律。

圖 | 團隊合影(來源:UIUC)
實驗的天選細胞——JCVI-syn3A
要在電腦裏模擬一個活細胞,是一項面臨生物複雜性挑戰的工作,所以首先要選擇一個足夠簡單的對象。而 JCVI-syn3A 正是這樣的存在。
它的前身可以追溯到 2010 年。那一年,J. Craig Venter 研究所(JCVI)合成了第一個完全由人工基因組驅動的細菌細胞 JCVI-syn1.0,基因組約 108 萬鹼基對、901 個基因。
2016 年,團隊將基因組精簡到 47.3 萬鹼基對、473 個基因,造出了 JCVI-syn3.0。它是已知自主複製生物中最小的基因組(據 Hutchison 等人 2016 年發表於《Science》的論文)。
但 syn3.0 有一個極大的缺陷:它不能正常分裂,細胞形態混亂。一直到 2021 年,JCVI 的 Pelletier 等人在 Cell 報道,通過加回 7 個基因(其中 5 個此前功能未知),這纔得到了 JCVI-syn3A:493 個基因,倍增時間約 105 分鐘,能規律地球形生長並對稱分裂。
493 個基因是什麼概念?大腸桿菌有大約 4,300 個基因,人類細胞有大約 2 萬個蛋白質編碼基因。Syn3A 可以說是自然界中能獨立存活的“最低配置”。正因爲足夠簡單,它成了全細胞建模的理想試驗場。
從“攪拌均勻”到真正的三維空間
Luthey-Schulten 團隊並非第一次做全細胞模型。2022 年,他們就在 Cell 上發表了 Syn3A 的“攪拌均勻”(well-stirred)模型,即把細胞當作一個均勻混合的反應器,用隨機-確定性混合動力學模擬基因表達、代謝和生長。那個模型已經能預測出與實驗吻合的倍增時間和蛋白質分佈。
但問題在於,細胞不是試管。RNA 聚合酶得在三維空間中擴散、找到 DNA 上的啓動子才能開始轉錄;負責降解 mRNA 的降解體(degradosome)被限制在細胞膜內側;核糖體有約 20 納米的體積,會擠佔周圍的空間。這些空間效應,在均勻攪拌的假設下全部被忽略了。
這次的 4DWCM 對這個侷限實現了全面突破。模型把細胞的三維空間切成了 10 納米邊長的立方格點,所有蛋白質和 RNA 都在格點上擴散、碰撞、反應……每一個分子都是獨立追蹤的粒子。這種空間上的異質性,使分子間的相遇與反應更貼近真實細胞內的擁擠環境,也自然呈現出生命過程固有的隨機特徵。
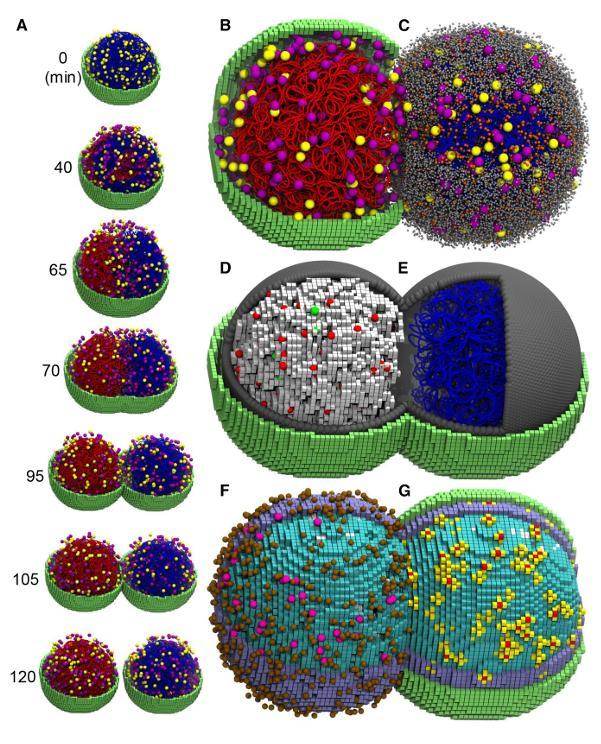
(來源:論文)
四種計算方法結合
不過要模擬一個細胞的全部過程,沒有哪一種計算方法能獨自勝任。因此團隊的做法是把四種不同的模擬方法組裝成一個混合框架:空間中的反應和擴散用 RDME(Reaction-Diffusion Master Equation,反應-擴散主方程)處理;全局的轉錄和 tRNA 裝載等反應用 CME(Chemical Master Equation,化學主方程)做隨機模擬;糖酵解、核苷酸合成等代謝網絡用 ODE(Ordinary Differential Equations,常微分方程)求解;染色體的物理行爲:聚合物運動、DNA 複製、蛋白驅動的環擠出,則用布朗動力學(Brownian Dynamics)在第二塊 GPU 上並行模擬。

(來源:論文)
四種方法通過一個通信算法每隔 12.5 毫秒同步一次數據。模擬一個完整細胞週期需要 4 到 6 天的實際計算時間。論文中報告的 50 個重複細胞模擬,總共消耗約 15,000 GPU 小時,全部運行在 NVIDIA A100 上。據 UIUC 新聞稿,團隊使用的是國家超級計算應用中心的 Delta 超算系統。
那麼通過這樣的方法“焊接”,最後模擬結果有多準?
最直接的驗證是倍增時間:模擬細胞平均 105 分鐘完成膜面積倍增,與實驗值完全一致。DNA 複製平均耗時 51 分鐘。
更精細的驗證來自 ori:ter 比,即染色體複製起點與終點的測序覆蓋深度之比,反映羣體中 DNA 複製的平均進度。模擬預測值爲 1.28,團隊自己做的全基因組測序實測值爲 1.21,高度吻合。這意味着模型不僅恢復了正確的總時間,連 DNA 複製的節奏也基本對了。
模型還預測了分裂時刻細胞的分子組成:約 881 個核糖體、176 個 RNA 聚合酶、192 個降解體。約 55% 的核糖體和 70% 的 RNA 聚合酶在任意時刻處於活躍狀態。mRNA 的平均半衰期約 3.6 分鐘,落在已知細菌的觀測範圍內。這些數字過去需要分別設計不同實驗去測量,現在從一次模擬中同時產出。
此外,4D 模型最有價值的地方,不是重複已有結果,而是揭示了空間效應對細胞行爲的實質影響。
一個典型例子:DNA 複製的啓動蛋白 DnaA 需要在三維空間中擴散到染色體的複製起點上,才能觸發複製。團隊最初使用的結合速率參數在 well-stirred 模型中工作正常,但在 4D 模型中,12 個測試細胞在 60 分鐘內無一啓動複製,因爲 DnaA 必須“真的走過去”纔行。換用了結合力更強的參數後,複製才正常啓動。在均勻攪拌假設下好用的參數,放到三維空間中可能就不夠了。
另一個發現涉及細胞分裂後的分子分配。核糖體、膜蛋白等的分配大致隨機,兩個子細胞之間沒有系統性偏差。但降解體出現了有趣的偏斜:當大塊 DNA 被擠向細胞一側時,DNA 佔據的空間會排斥附近的降解體,導致那一側降解體偏少。這種空間擁擠導致的不均勻分配,是把細胞當試管的模型永遠看不到的。
不過,實驗也存在其侷限性。最突出的一個:染色體分離靠的是人工施加的排斥力。Syn3A 基因組中找不到已知的染色體分離系統,團隊不得不用外力“推開”兩條子代染色體。論文承認這是一個限制,初步探索顯示更精細的蛋白模型可能有潛力替代,但計算成本太高,可能把單個細胞的模擬時間從 6 天拉到數週。
其他侷限還包括:沒有處理多個基因共轉錄的情況;缺少多核糖體效應(多個核糖體同時翻譯一條 mRNA),導致長蛋白質產量偏低;代謝中某些核苷酸的濃度偏低,可能缺少反饋抑制機制。團隊也列出了下一步最需要的實驗數據:Syn3A 的定量代謝組學、全基因組 mRNA 半衰期、蛋白質半衰期、以及長讀長轉錄組學。
全細胞建模的一個臺階
此次的研究還帶領全細胞建模走上了一個新臺階。
此前最有影響力的全細胞動力學模型是 2012 年的生殖支原體模型(Karr 等,Cell)和 2020 年的大腸桿菌模型(Macklin 等,Science),將細胞內部視爲均勻混合體系,未納入空間維度的影響。
而本次針對 Syn3A 構建的 4DWCM 框架,首次實現了空間分辨率、反應隨機性與完整細胞週期三者的同步整合,使模型能夠更真實地反映分子在細胞內的定位、擴散與相互作用過程。不過背後的代價是巨大的算力消耗。
團隊指出,未來兩種模型應該形成互補:用 4D 模型校準參數,再用 well-stirred 模型做大規模採樣。這種分層建模策略,有望在保持物理真實性的同時,提升全細胞模擬的實用性與可擴展性。
參考鏈接:
1.https://www.cell.com/cell/fulltext/S0092-8674(26)00174-1
運營/排版:何晨龍





