科學家把一組被基因改造的早衰症(progeroid)小鼠放進一套磁通密度 2.0 mT、頻率 60 Hz 的極低頻電磁場(ELF-EMF)裏,按“開 3 天、關 4 天”的節奏循環曝照 90 天。實驗結束時,這隻本該在幾個月內死於加速衰老的小鼠比對照組多活了十幾周,毛髮由稀疏變得密實,血管外膜變薄,肝臟和腎臟裏 p21、Atf3、Il6、Ccl2 這些衰老標誌基因的表達被壓下一半以上。
但如果調整參數,不再採用“開 3 天、關 4 天”的節律,而是連續打開 14 天不休息,同樣的小鼠會表現出很差的耐受性,死亡和體重下降都明顯增加。
這組對比來自韓國東國大學 Jongpil Kim 團隊近期發表於《細胞》(Cell)的一篇題爲《電磁場誘導型體內基因開關,用於基因表達的遠程時空控制》(Electromagnetic field-inducible in vivo gene switch for remote spatiotemporal control of gene expression)的研究。論文通訊作者是 Kim,合作方包括賓夕法尼亞大學、韓京國立大學。他們想做的,是把磁場變成人體內基因表達的遙控器。

圖丨相關論文(來源:Cell)
過去二十年,生物學界一直在找更好的辦法遠程啓動或關閉一段基因的表達。藥物誘導(最常見的是四環素 Tet-On/Off 系統)、光誘導(光遺傳學)、熱誘導(熱休克蛋白啓動子)、超聲誘導這幾種方案都各自有自己的硬傷,藥物有脫靶反應和代謝時間差,光穿不透深層組織,熱和超聲的時空精度都不夠。相比之下,磁場看上去好像要更理想一點:沒有組織穿透障礙,不留下物質殘留,能幾乎瞬時通斷。但問題在於,細胞憑什麼“感覺”到磁場?
2015 到 2016 年前後,洛克菲勒大學、弗吉尼亞大學等幾家實驗室在 Science、Nature Medicine 等期刊連續發表“磁遺傳學”(magnetogenetics)工作,方法是把鐵儲存蛋白 ferritin(鐵蛋白)與溫度或機械敏感的離子通道(TRPV4、TRPV1)融合,號稱施加磁場就能讓通道打開、讓神經元放電,甚至控制小鼠的進食行爲。論文一出,一度轟動。
但緊接着,質疑聲也隨之而來。加州理工學院神經生物學家 Markus Meister 在 eLife 上發了一篇接近教科書級別的物理分析:按照已知的鐵蛋白磁性和離子通道能量尺度,磁場和這套融合蛋白的相互作用能量,比細胞內時時刻刻存在的熱漲落小了 5 到 10 個數量級。換句話說,隨機的熱擾動能量遠大於磁場能提供的“推力”,這套機制在物理上根本不成立。
物理層面的反對之外,2019 到 2020 年至少有三個獨立實驗室報告,他們用完全相同的方法(Magneto2.0)重複不出原始論文裏的神經元激活效應。磁遺傳學一度陷入“有人看得到、有人看不到”的尷尬。後續研究提出一種間接路徑:磁場讓 ferritin 內部的鐵離子重分佈,生成活性氧(ROS),ROS 再觸發下游信號,但其精度和可靠性仍然有限。
Kim 團隊這次繞開了 ferritin 路線。他們的起點是一個十年前埋下的舊問題:2014 年他們團隊在 ACS Nano 發表的一項研究顯示,大約 50 赫茲的極低頻磁場能讓成體細胞被重編程爲多能幹細胞的效率提升幾倍,但當年沒搞清楚細胞究竟通過哪一個分子感知了磁場。十年之後,他們決定從頭篩一遍:做全基因組 CRISPR-Cas9 敲除篩選,把兩萬多個基因挨個敲掉,看哪一個被敲掉會讓磁場開關失效。
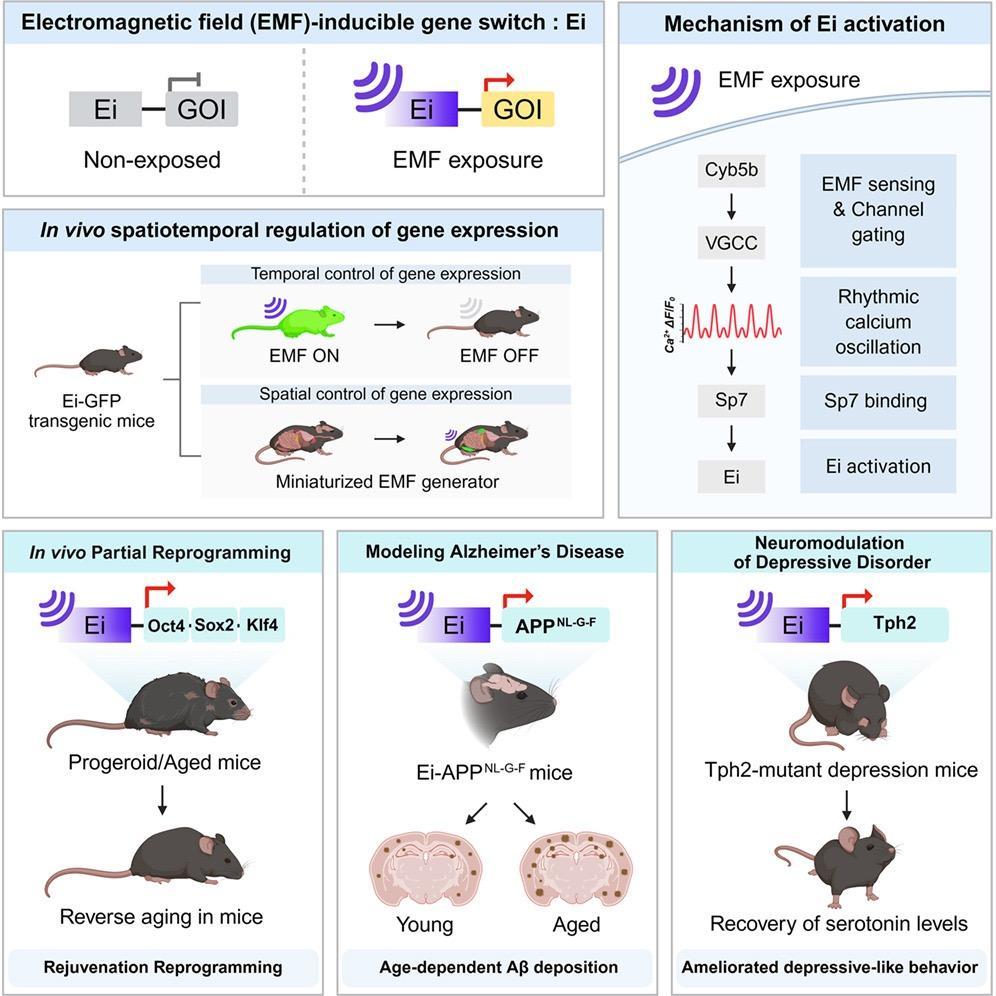
圖丨圖示摘要(來源:Cell)
他們先構建了一種報告細胞:在小鼠成纖維細胞裏裝入一段事先識別出的 Lgr4 啓動子片段(後來被定義爲 Ei 元件,約 450 個鹼基),下游接綠色熒光蛋白(GFP)。這些細胞暴露在 2.0 毫特斯拉、60 赫茲的磁場下會亮起來。
向這批細胞池裏引入覆蓋 20,611 個基因、每基因 6 條 sgRNA 的慢病毒文庫,讓每個細胞被隨機敲掉一個基因。打開磁場,有些細胞依舊能亮,有些不再亮。對後者富集的 sgRNA 做測序,那些被敲掉的基因就是磁場信號通路上的關鍵節點。
篩選裏最顯著的一個命中基因是 Cyb5b(cytochrome b5 type B,細胞色素 b5 B 型),這是一種位於線粒體外膜的電子載體蛋白,此前和磁場沒什麼關聯。敲掉它,開關幾乎完全失活;補回來,敏感性立刻恢復。
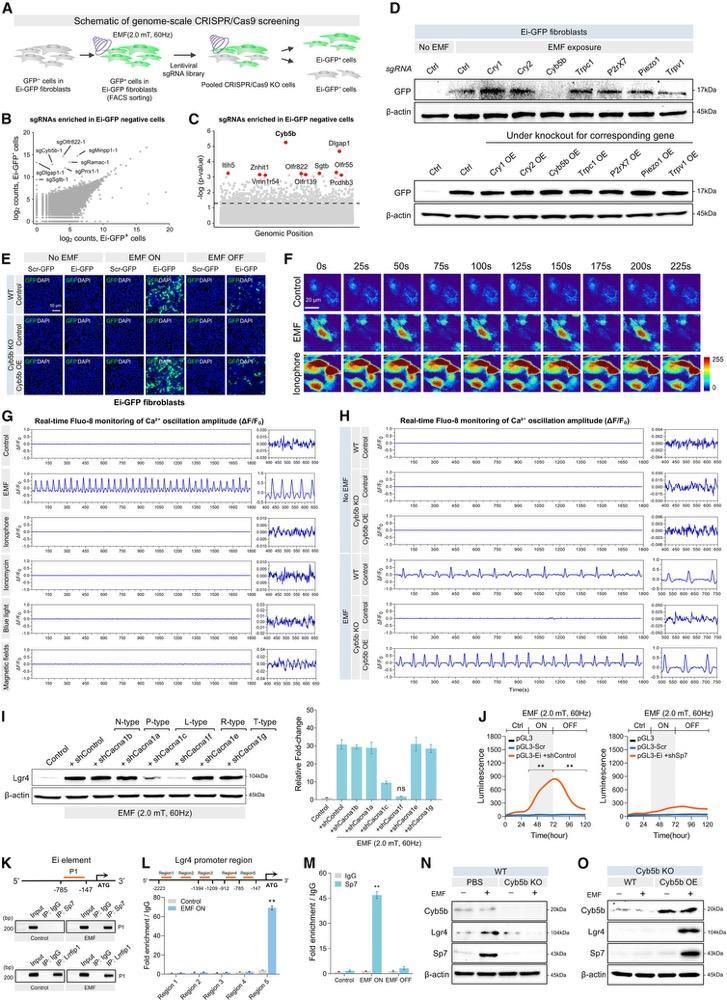
圖丨電磁場誘導基因開關激活的 Cyb5b 依賴性機制(來源:Cell)
之後他們進一步拆解信號鏈。磁場暴露下,細胞質裏的鈣離子濃度出現一種特殊波形:精確、重複、和磁場週期同頻的小幅振盪;而藥物激動劑誘發的鈣響應通常是一次起伏較大的緩慢湧入,兩者形態完全不同。
這種機制在神經科學裏被稱爲“頻率編碼”:同樣是鈣信號,節奏不一樣,細胞給出的下游反應就不一樣。磁場改變 Cyb5b 的氧化還原狀態,後者調節一種 L 型鈣通道(Cacna1f)的門控,讓鈣離子按磁場節律進出;鈣振盪進一步激活轉錄因子 Sp7,Sp7 再結合到 Ei 元件上,啓動下游基因表達。
磁場→基因表達這條分子鏈條由此被完整拼起。和此前的磁遺傳學方案不同,鏈條上每一步都依賴細胞裏本來就有的、可重複鑑定的蛋白,而不是外掛的合成納米粒子。
有了可工作的系統之後,團隊選了三個方向做活體驗證。
三組裏最直觀的是抗衰老。團隊把 Ei 元件接在 Oct4-Sox2-Klf4 這三個山中因子(Yamanaka factors,誘導多能幹細胞的經典組合,去掉了容易致癌的 c-Myc)前面,做成 Ei-OSK 病毒,注入老年或早衰小鼠。短暫表達這三個因子可以把衰老細胞“年輕化”,這即是近年抗衰老領域最熱的賽道“部分重編程”(partial reprogramming)。
部分重編程的難點在於,這三個因子如果連續表達,細胞會徹底丟掉原有身份,帶來畸胎瘤和增生風險。藥物誘導系統開關速度跟不上,光和熱穿不到深層器官,讓這件事在活體動物上一直難以安全執行。
磁場誘導在這裏提供了新的解法:3 天開、4 天關的節律,讓 OSK 表達足夠高到能抹除衰老印記,又低到讓細胞守住自己是成纖維細胞、皮膚細胞還是血管細胞的身份。早衰症小鼠的存活曲線被明顯抬升,體重穩定,血管外膜變薄,皮膚傷口兩週內膠原堆積減少近一半。
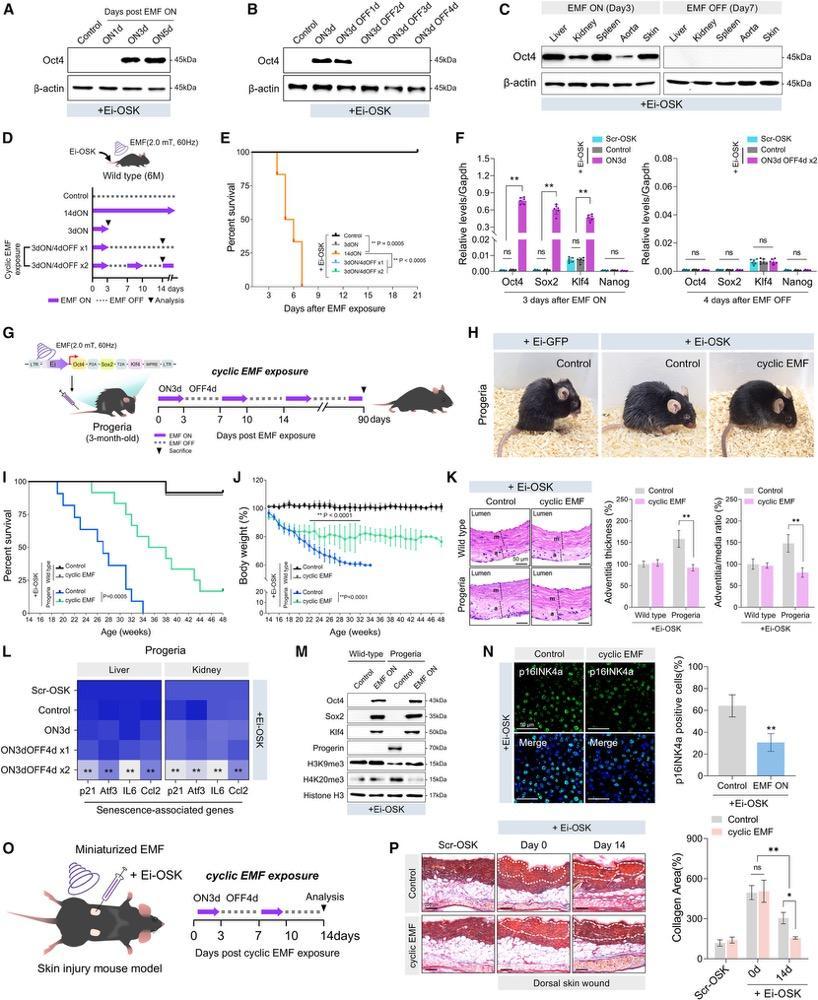
圖丨通過電磁場(EMF)誘導的 OSK 基因開關進行體內部分重編程(來源:Cell)
第二組驗證換到了阿爾茨海默病(AD)上。傳統 AD 小鼠從出生起就過量表達突變型 APP 蛋白,子宮裏就開始堆積 β 澱粉樣蛋白(Aβ),和人類散發性 AD(病理往往在幾十年後纔出現)在時間軸上嚴重錯位。Kim 團隊把 Ei 接在人類突變型 APP 基因前面,得到的 Ei-APP 小鼠只有在接受磁場暴露時纔開始表達致病 APP。
研究者可以選在小鼠 3 月齡(相當於年輕人)或者 20 月齡(相當於老年)時才“打開”病理。這是第一次在小鼠上看到年齡依賴的 Aβ 沉積,年輕小鼠幾乎沒有斑塊,老年小鼠皮層和海馬區大面積沉積,配套出現膠質細胞激活和記憶、空間辨別任務上的明顯缺陷。這一步讓“腦衰老本身的作用”和“Aβ 毒性的作用”第一次有機會被分開來研究。
第三組是抑鬱症相關的血清素調控。Tph2-KI 小鼠因爲色氨酸羥化酶基因突變,5-羥色胺合成不足。研究者把野生型 Tph2 接在升級版的 sEi 元件下面(加了 CMV 增強子,反應更快),立體定向注射到大腦的背側中縫核。然後兩種曝照方式做對比:每天照 12 小時(模擬生理節律)對每天照 24 小時。結果只有節律性 12 小時那組的抑鬱樣和焦慮樣行爲得到恢復,連續曝照反而沒效果。
這一結論說明,血清素系統需要可能的不是一個持續被打開的閥門,而是一個跟着晝夜節奏開關的龍頭。現有基因療法大多是“恆開”模式,對需要節律的神經系統反而並不適配。磁場遙控恰好給了節律控制的可能。
空間精度和長期安全性是工程層面的另外兩個關注點。團隊做了微型化磁場發生器,貼在頭顱、胸部、腹部或骨盆不同位置,讓 Ei 開關只在對應器官被打開,周圍組織幾乎不響應,全身暴露缺乏空間精度的問題被部分解決。長期安全性上,野生型小鼠在同樣的磁場條件下連續暴露 6 個月,神經、肝、腎功能指標,血液學檢測,多器官轉錄組分析都沒看出應激響應或所謂“電磁場敏感”標誌物的異常。
這樣一套系統要產生效果,需要同時滿足特定頻率、特定強度、特定脈衝波形、特定暴露時長,還得先把 Cyb5b 表達結構和 Ei 元件植入到細胞裏。
說起來,這些條件乍一聽很容易讓人聯想到長期活躍在互聯網的那些陰謀論,比如“電磁場控制大腦”、“基站改變基因表達”等等。事實上,這篇論文發表後,社交媒體上圍繞它的討論裏確實出現了不少這類聯想,比如“住在變電站旁邊對身體有影響原來是真的”,或者擔心“以後可以隨意激活或關閉特定基因”等等。
但實際上,Kim 團隊這項工作其實反而證明了,細胞要對電磁場做出可控的基因反應,門檻極高。現實裏的磁場想改變基因表達,不是走進一個 Wi-Fi 覆蓋區或者經過一根高壓線就能發生的事。
科學家花幾十年研究,用 CRISPR 全基因組篩選、分子機制解析、病毒載體遞送、活體實驗驗證一整套工具才做到按磁場節律開關一個基因。那些陰謀論者認爲只靠電磁場就輕易改變基因,哪有這種好事?
且這套系統目前只在小鼠身上跑通。一副能均勻覆蓋小鼠全身的亥姆霍茲線圈,搬到人身上就是另一個工程問題,腹腔深處或腦區要維持同樣精確的磁場參數,尺寸、能耗、均勻度都不在一個量級。病毒載體的遞送效率、免疫反應和脫靶整合,也是基因治療領域從小鼠走向人時要重新面對的一整套難題。至於安全性,6 個月的連續暴露在壽命約兩年的小鼠身上已經算長期觀察,換到壽命長几十倍的人身上,這個窗口遠遠不夠。
還有一層不確定性在機制本身。Cyb5b 是篩選裏最顯著的命中基因,但這種位於線粒體外膜的電子載體蛋白究竟怎麼把磁場這種物理信號翻譯成下游的鈣振盪,論文給出的氧化還原 - 鈣通道門控模型仍然屬於機制假說,細節需要結構生物學和生物物理層面的獨立工作來補充。磁遺傳學當年栽跟頭,就是因爲機制解釋經不起物理層面的推敲。
Kim 在論文裏把這套系統稱作“通過生物學解碼電磁場的高度可調平臺”。比起十年前磁遺傳學高調登場又迅速退潮,這一次有全基因組篩選出的分子機制、三類獨立的活體驗證和 6 個月的安全性窗口,起點確實清晰得多。至於它會不會重蹈前輩們的覆轍,還有待時間驗證。
參考資料:
1.https://doi.org/10.1016/j.cell.2026.03.029
2.https://doi.org/10.7554/eLife.17210
3.https://doi.org/10.1523/JNEUROSCI.1717-23.2024
4. https://pubmed.ncbi.nlm.nih.gov/25248035/
運營/排版:何晨龍





